トピ ロキソ スタット - トピロキソスタット(ウリアデック ・トピロリック)の作用機序・特徴・強さの比較【ファーマシスタ】薬剤師専門サイト
フェブリクとトピロリックの違いは?
人により副作用の発生傾向は異なります。
(保管上の注意) 室温保存。
*)〔8. 本剤と併用する場合は、キサンチン系薬剤の投与量に注意すること。
2. 肝機能障害があらわれることがあるので、本剤投与中は定期的に検査を行うなど患者の状態を十分に観察すること〔11. ウリアデック/トピロリック(トピロキソスタット)はフェブリク(フェブキソスタット)に次ぐ、選択的XOD阻害薬。
トピロキソスタット(ウリアデック ・トピロリック)の作用機序・特徴・強さの比較【ファーマシスタ】薬剤師専門サイト
腎機能低下 患者では? 軽度及び中等度 腎機能低下には 通常量可 軽度及び中等度 腎機能低下には 通常量可 腎機能障害 減量を等を考慮 とまぁ、 フェブリクに完敗・・。
その後は血中尿酸値を確認しながら必要に応じて徐々に増量する• 73㎡未満• 本剤もキサンチンオキシダーゼ阻害作用をもつことから、同様の可能性がある。
214• 高齢者 65歳〜• キサンチンオキシダーゼが存在するために尿酸が作られます。
それでは、このキサンチンオキシダーゼの働きを抑えてしまえば、尿酸の産生が抑制されるはずです。
トピロリック、ウリアデック(トピロキソスタット)の作用機序:痛風・高尿酸血症治療薬
なお、トピロキソスタットの代謝・排泄には主に肝臓が関わっているため、腎臓の機能が低下してしまった患者さんに対しても使用することができます。
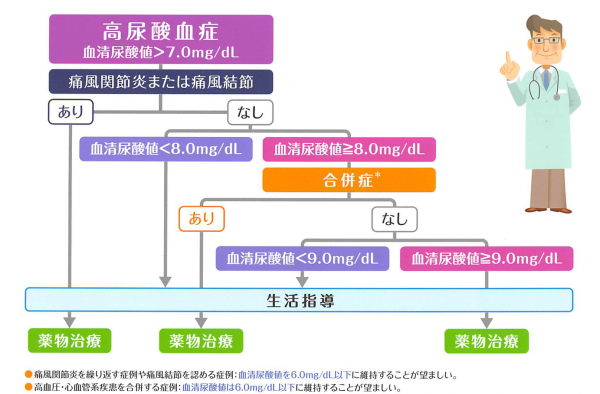
47 ガイドラインでは、無症候性の場合、高血圧、心疾患、糖尿病、メタボなどの心血管リスクとなる疾患がある場合は尿酸値8. (40代診療所勤務医、代謝・内分泌内科)• その後、血中尿酸値を確認しながら必要に応じて増量。
作用機序 キサンチン酸化還元酵素に競合的に阻害し、尿酸生成を抑制する。
0%(54/60例)であった。
トピロキソスタット(ウリアデック ・トピロリック)の作用機序・特徴・強さの比較【ファーマシスタ】薬剤師専門サイト
通常、成人にはトピロキソスタットとして1回20mgより開始し、1日2回朝夕に経口投与する。
一応トピロリック・ウリアデックの基本情報もまとめときます。
・腎障害がある痛風患者にも、比較的安全に処方できる。
そして、これら合併症を有する患者に対しても、尿酸値低下が心血管障害リスクを減少するかは十分なエビデンスがないと記載されている。
フェブリクとウリアデックの違い
2歳の息子と妻の3人家族。
その後は血中尿酸値を確認しながら必要に応じて徐々に増量する。
過敏症• 承認時までの国内の臨床試験では、35. (授乳婦) 治療上の有益性及び母乳栄養の有益性を考慮し、授乳の継続又は中止を検討すること(動物実験(ラット)で乳汁中への移行が報告されている)。
ウリアデックが三和化学で、トピロリックが富士薬品。
トピロリック・ウリアデックとフェブリクとザイロリックの比較。
痛風を含む高尿酸血症患者(157例)を対象として、プラセボ対照二重盲検並行群間比較試験を行った。
1983年11月 岡山県倉敷中央病院で生まれ、水の都である愛媛県西条市で育つ。
心血管死の中では両群ともに心突然死が最も多かった(フェブキソスタット群2. (小児等) 小児等を対象とした臨床試験は実施していない。
血清尿酸値の変動は痛風関節炎を引き起こす原因になるため、日内変動が少ないほうが尿酸コントロールに適しているということです。
リアルレポート|第12回 尿酸生成抑制薬3剤における3つの違い|三和化学研究所
アロプリノール、トピロキソスタットについてはウリアデックのインタビューフォームから、フェブキソスタットはフェブリクのインタビューフォームから抜粋しています。
一方、ウリアデックやフェブキソスタットは肝臓で代謝され、糞・尿中に排泄されるため、 軽~中等度の腎機能障害があっても減量の必要はありません。
また、全ての副作用が明らかになっているわけではありません。
トピロキソスタットはハイブリッド型? トピロキソスタットはフェブキソスタットとアロプリノールのそれぞれの特徴を併せ持った「ハイブリッド型」と言われる。
医療用医薬品 : トピロリック (トピロリック錠20mg 他)
73㎡未満)を対象とした有効性及び安全性を指標とした臨床試験は実施していない。
重大な副作用として添付文書に記載されているものは、肝機能障害 2. 社内資料:ラットにおけるクエン酸塩の影響の検討(承認年月日:2013年6月28日、CTD 2. 210• 尿酸は新しく作られたり、尿と一緒に排泄されたりを毎日繰り返しています。
ウリアデックは血清尿酸値を治療目標値(6. 維持量は通常1回60mgを1日2回とし、患者の状態に応じて適宜増減するが、最大投与量は1回80mgを1日2回とする。
その後は血中尿酸値を確認しながら必要に応じて徐々に増量する。
- 関連記事
2021 tmh.io