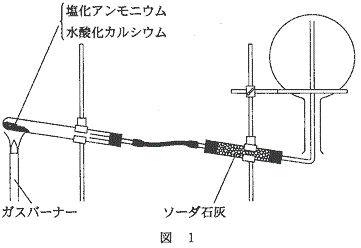
塩化 アンモニウム 水 酸化 カルシウム - 塩化 アンモニウム と 水 酸化 カルシウム
塩の加水分解|化学基礎【高校化学Net参考書】
水酸化カルシウム(すいさんかカルシウム、Calcium hydroxide)は、 Ca OH 2 で表されるの。
その結果、フラスコないが真空となり、 フェノールフタレイン溶液が噴水のように飛び出す。
パウダー状 顆粒状 ・パウダー状で固結しにくい ・吸水性がある(無水) ・粒度調整ができる 塩化カリウム KCl 清涼飲料水 調味料 人工透析の原料 カラギナンの増粘剤 洗剤 メッキ助剤 グラウト剤 フラックス剤 局方 食品添加物 肥料 飼料添加物 自社規格品 商品によって25kgと20kgがあります。
そのため、2007年11月にスポーツ・青少年局学校健康教育課長名で通達 が出されたこともあり、白線用としては、より安全なに変更されている。
塩化アンモニウムと水酸化カルシウムを混ぜそれを加熱するとアンモニア水...
なんか、イオンとか関係あるんでしょうか? 非常にややこしいです。
でも疑問に思うのはそのことではありません。
呼吸困難• 化合 かごうの化学反応式一覧 化合とは:2種類以上の物質が結びついて、別の1種類の物質ができる化学変化のこと。
8程度と高いためとして分類されるが、溶解度はなどの水酸化物よりはるかに低く、塩基としての作用はこれらより弱い。
塩の加水分解|化学基礎【高校化学Net参考書】
中和反応として考えるのであればNH4+からOH-にH+が移っていますからNH4+が酸、OH-が塩基であるとすればいいです。
工業的歴史 [ ] ソルベイ法が実用化される以前に利用されていた炭酸ナトリウムの工業的生産法としてはがあった。
弱酸が電離して生じた陰イオンの一部は,水素イオンと反応して元の酸に戻ります。
Ca(OH)2は強塩基です。
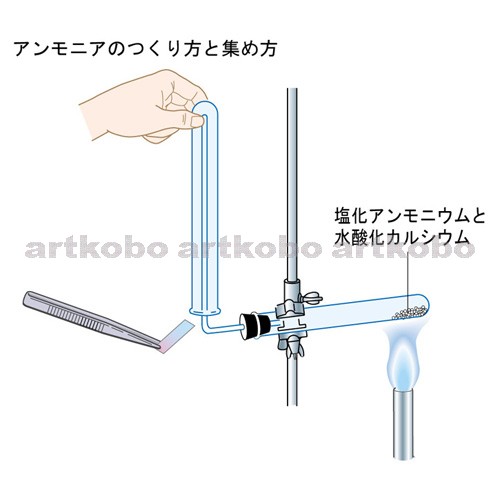
3分でわかるアンモニアの発生方法
現代でも、やなどの防疫のため、消石灰が利用されている。
「 塩の元の酸・塩基の強弱(電離度)に差がある場合,強い方の性質が表れる」というまとめ方が一般的です。
乾燥剤と気体が中和反応を起こすような組み合わせは不適であるわけです。
酢酸ナトリウムは酢酸(弱酸)と水酸化ナトリウム(強塩基)からなる塩で,その水溶液は塩基性です。
塩化 アンモニウム と 水 酸化 カルシウム
これは「二酸化炭素と石灰水が反応して、水にとけない白い沈殿ができた」という状況です。
しかし,硫酸水素イオンHSO 4 -はさらに電離して水素イオンを生じます。
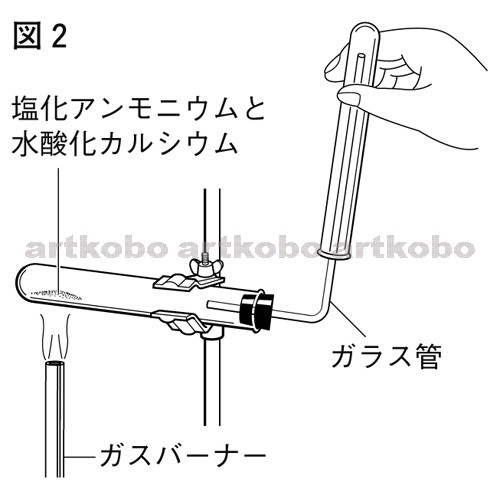
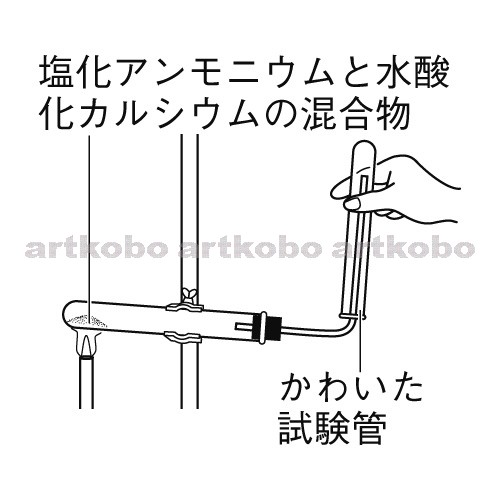
アンモニアの実験室的製法は、どの参考書にも、 「塩化アンモニウムと水酸化カルシウムの固体同士を加熱する」と書かれています。
・ 水に溶けると アルカリ性を示す。
塩化アンモニウム+水酸化カルシウム
回答お願いします。
または中性の・としても使われる。
その際、塩化ナトリウムが 塩 えんとして生成される。
水酸化カルシウムは強塩基であり、微生物の繁殖を抑制したり不活性化する性質がある。
- 関連記事
2021 tmh.io