塩化 アンモニウム 水 酸化 バリウム - 第27章 塩の性質
12125
4 112 162 178 97 102 108 113 125 178 62. (4)生徒実験 (12分~20分) 2つの実験を行います。
においても、硫酸塩の分析には塩化バリウムを用いた比濁法もしくは重量法が採用されている。
高校の物理や化学程度の知識はありますが、 理科系の高等教育は受けていないという前提でお答えしますね。
皮膚に付着した場合 多量の水と石けん 鹸 で洗うこと。
塩化 アンモニウム 水 酸化 バリウム
6 313 337 361 398 471 580 658 16. 急性症状及び遅発性症状の最も重要な徴候症状 情報なし 応急措置をする者の保護 救助者は、状況に応じて適切な保護具を着用する。
十分に事前学習させてください。
ミョウバンは硫酸カリウムアルミニウム十二水和物AlK SO 4 2・12H 2Oですが,硫酸カリウムアルミニウムAlK SO 4 2は複塩です。
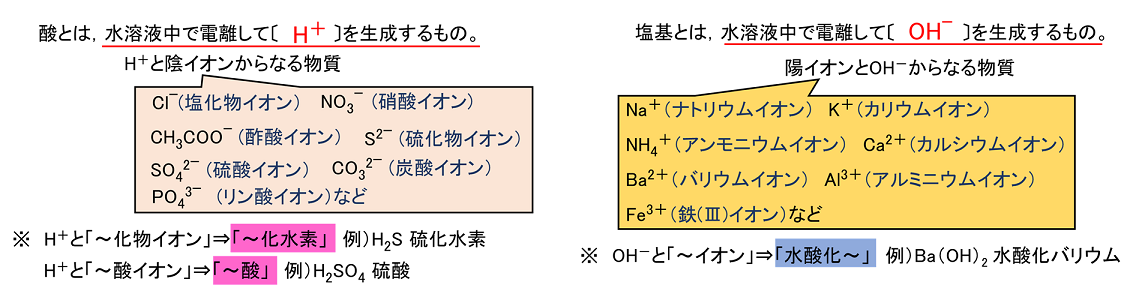
国際規制 国連番号 1564 国連品名 BARIUM COMPOUND, N. ファイル• 上がる• 塩基性塩 塩基のOH -が残った塩(水溶液が塩基性を示すということではない) Cu OH Cl 塩化水酸化銅など 名称に「・・・水酸化~」となる。
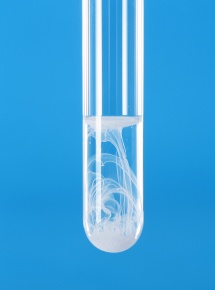
アンモニアの発生と吸熱反応(塩化アンモニウムと水酸化バリウム)
すなわち,水溶液中のナトリウムイオンと水酸化物イオンの濃度は変化しないということです。
8 114 144 58 98 120 149 200 154 166 179 198 221 269 308 329 355 3. 安全な容器包装材料 破損や漏れの無い密閉可能な容器を使用する。
例えば、塩化バリウムを水酸化ナトリウムなどを用いて複分解させることで純粋な水酸化バリウムが生成される。
塩酸は揮発性の酸です。
12125
危険有害反応可能性 通常の取扱い条件下では危険有害反応を起こさない。
ただし,[イ]には気体が,[エ]には液体が入ります。
1 110 200 414 113 134 112 138 175 83. 水を加えてから電子てんびんに載せておけば、アンモニアの発生、質量の変化などが一目瞭然で分かる。
特有の危険有害性 火災等の場合は、毒性の強い分解生成物が発生する可能性がある。
塩化 アンモニウム 水 酸化 バリウム
化学的安定性 通常の取扱い条件下では安定である。
15.適用法令 法規制情報は作成年月日時点に基づいて記載されております。
6 216 233 256 283 324 350 381 398 37. 1.食塩が水に溶けるときの反応 NaClが水に溶けるとき、次の反応が起きます。
・弱塩基の塩に強塩基を加えると,強塩基の塩ができて弱塩基が遊離する。
実験20 吸熱反応/2年理科/takaの授業記録2017
4 下線部「 ぬれたろ紙をかぶせ」ることで,アンモニアが発生した時の刺激臭をおさえることができます。
吸収された熱エネルギーは化学エネルギーとなってどうなったのですか? 質問が多くてすみません。
分析用試薬として、主にpH緩衝剤として試液に汎用される。
Kaye and Laby Online• ということは,水溶液中の水素イオンH +と酢酸イオンCH 3COO -が結びついて,酢酸分子CH 3COOHになりやすいことを意味しています。
- 関連記事
2021 tmh.io