窒素 原子量 - 水、水素、酸素、窒素などの分子量一覧まとめ
化合物の原子量表2020
不確かさは有効数字の最後の桁に対応する。
左端から1s、2s(二分割し内部構造を露出させている)、2p x、2p y、2p z 軌道である。
亜硝酸塩は安定で種々の塩が知られている。
今度は水素原子の数を求める問題です。
物質量
そのため,当該元素の原子量が表記の値とかなり異なることがある。
これからの計算問題は全てと言って良いほどこのmolを使って mol = mol の関係式で解いていきます。
4:原子量の計算問題 最後に、原子量の計算問題を1つ解いてみましょう。
(注)飲料水中の硝酸塩は,特に乳幼児のメトヘモグロビン血症との関連や,ヒトにおける心血管系や副腎への影響,糖尿病との関連,母親の妊娠中の曝露による生殖への影響や子どもの中枢神経系の先天奇形,腫瘍との関連を示唆した疫学研究がある。
原子量とは?求め方や単位も見やすい図と例で即理解!分子量との違いも|高校生向け受験応援メディア「受験のミカタ」
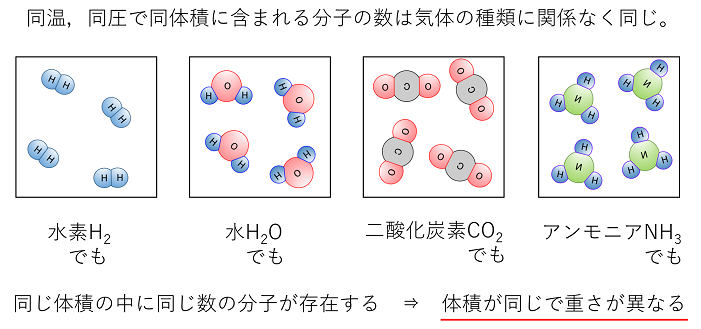
もっとややこしい分子でも同じです。
今までは比例式を主役にしてきましたがこれからはちょっと変えていきますよ。
硫安の袋に記載されている窒素21%は、硫安分子 132 の中の窒素 28 の割合を示しています。
分子も相対質量なので 単位はありません。
窒素の分子式と構造式は?窒素の質量と密度[g/cm3]や分子量の計算方法【1立方メートルの重さ】|モッカイ!
硫酸ナトリウムNa 2SO 4 1mol中に硫酸イオンSO 4 2-は1mol含まれるので、今硫酸イオンは0. そして物質量の比は分子数の比になることも考えると、適当な数値を選んで計算すればいいとわかります。
) この問題は「この溶液全体の分子」となるので 水分子も計算しなくてはいけません。
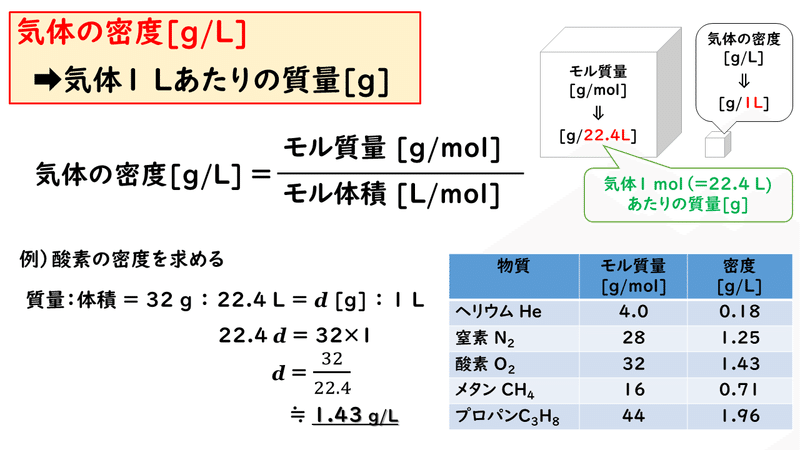
密度1. 具体的には、1L=1000cm3であるため、上の数値を1000で割るとよく、空気の密度は0. 0、酸素16なので分子量は180となります。
ただし、アボガドロ定数は 6. 式量に g をつければ 1mol の質量になるので 「 1mol で 286g なら 0. N原子には同位体という物が複数存在し、同じように陽子を7つもつN原子でも、質量の違う物が複数混在しています。
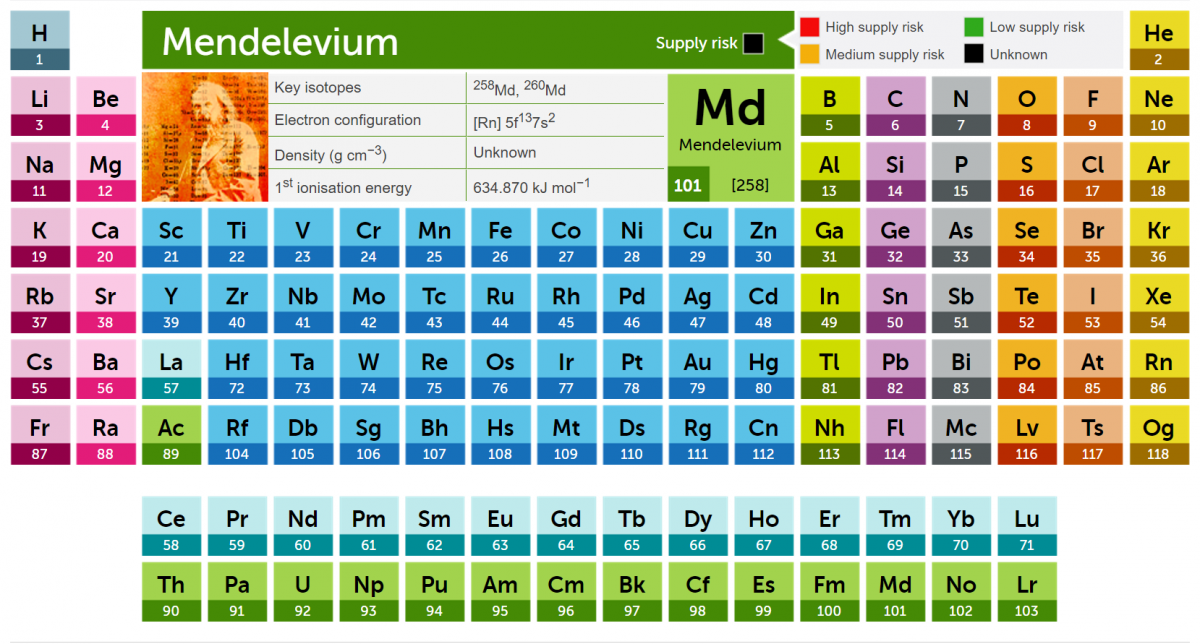
原子量
まずはこちらからご連絡ください! ポイント• 現実の気体も、通常の圧力、温度の範囲内では「理想気体」とみなせます。
「何だか一般的じゃない」と思う人は質量を文字を使って解いておくと良いです。
式量も相対的な値になりますので単位はありません。
硫黄32、酸素16として硫酸イオンの式量を自分で計算してみて下さい。
窒素の分子式と構造式は?窒素の質量と密度[g/cm3]や分子量の計算方法【1立方メートルの重さ】|モッカイ!
(なぜ、考えるかと言うとN原子の平均的な質量を決定することが重要だからです)。
原子量と分子量 分子を構成する原子の種類と数を元素記号で表した式を 分子式といいます。
計算は続きますので分数のままにしておきましょう。
N原子の陽子の数は7つで、N2分子の陽子数合計が14になることは、あなたの考えの通りです。
質量や原子数分子数と物質量(mol)を変換する計算問題
化合物の原子量表2020 (元素の原子量は,質量数12の炭素( 12C)を12とし,これに対する相対値とする。
m:不詳な,あるいは不適切な同位体分別を受けたために同位体組成が変動した物質が市販品中に見いだされることがある。
すると、ショ糖は 1mol、水は 19mol、となります。
: dinitrogen• つまり46%以外の54%は、炭素 C 、酸素 O 、水素 H となります。
物質量
5 となります。
どういうことかと言うと、 molは計算できて当たり前で、それを使って化学の計算問題は解いて行く、ということです。
原子量は相対値なので、基本的には単位はありません。
例えば、H 2Oの分子量を考えてみましょう。
- 関連記事
2021 tmh.io